

Сила скупљања било које дужине јединице на површини течности назива се површинска напетост, а јединица је Н. · М-1.

Имовина смањења површинске напетости растварача назива се површинским активностима, а супстанца са овом некретнином назива се површинска активна супстанца.
Површинска активна супстанца која може везати молекуле у воденом раствору и формирати мицеле и друга удружења и имати високу површинску активност, а истовремено има и ефекат влажења, емулгирања, пењења, прања итд. Назива се површински активно средство.
Сурфактант је органска једињења са посебном структуром и имовином, која може значајно променити међусобну натезање између две фазе или површинске напетости течности (углавном воде), са влажним, пенањем, емулгацијом, прања и других својстава.
У погледу структуре, сурфактанти имају заједничку карактеристику у којој у својим молекулама садрже две групе различитих природних природних. На једном крају је дугачак ланац непарске групе, растворљив у нафту и нерастворљивим у води, такође познат и као хидрофобна група или водооткривена група. Таква водоотпорна група је генерално дуге ланци угљоводоника, понекад и за органски флуорински, силицијум, органофосфат, органотни ланац итд. На другом крају је група растворљива у води, хидрофилна група или нафтна-рефетентна група. Хидрофилна група мора бити довољно хидрофила како би се осигурало да су цела површински активна средства растворљива у води и има потребну растворљивост. Пошто сурфактанти садрже хидрофилне и хидрофобне групе, могу се растворљиви у најмање једној од течних фаза. Ова хидрофилна и липофилна имовина површински активно средство назива се амфифичност.


Сурфактант је врста амфифилне молекула са хидрофобним и хидрофилним групама. Хидрофобне групе површински активних средстава углавном су састављене од дугорочних угљоводоника, попут равног ланца алкил Ц8 ~ Ц20, разгранати ланац алкил Ц8 ~ Ц20, алкилфенил (алкил угљен Том број је 8 ~ 16) и слично. Разлика која је мала између хидрофобних група углавном је у структурним променама угљоводоничних ланаца. А врсте хидрофилних група су више, тако да се својства површински активних средстава углавном односе на хидрофилне групе поред величине и облика хидрофобних група. Структурне промене хидрофилних група су веће од оних хидрофобних група, тако да се класификација површински активних средстава углавном заснива на структури хидрофилних група. Ова класификација се заснива на томе да ли је хидрофилна група јонска или не, и подељена је на анионски, катионски, неионички, зВиртион и друге посебне врсте површински активних средстава.

① адсорпција површински активних средстава на интерфакту
Молекули површински активна средства су амфифилни молекули који имају и липофилне и хидрофилне групе. Када је површински активно средство растворено у води, његова хидрофилна група привлачи воду и раствара се у води, док је њена липофилна група одбијена водом и оставља воду, што је резултирало адсорпцијом молекула површински активне материје (или јонима) на интерфејсу две фазе, што смањује интерфејс две фазе. Више молекула површински активне површине (или јоне) се адсорбује на интерфејсу, то је веће смањење интерфацијске напетости.
② Неке особине адсорпције мембране
Површински притисак адсорпционе мембране: површински активна средства на гас-ликвидном интерфејсу да би се формирао адсорпциона мембрана, као што је преносни плутајући лист без трења, плутајући лист гура мембрану Адсорбент дуж површине раствора, а мембрана ствара притисак на плутајућим лим.
Површинска вискозност: попут површинског притиска, површинска вискозност је имовина која је изложена нерастворљивим молекуларним мембраном. Суспендују фином металном жицом Платинум прстена, тако да његов авион контактира водену површину резервоара, закрените прстен за платине, платинасти прстен вискозности ометања воде, амплитуда постепено пропада, према којој се може мерити површинска вискозност. Метода је: Прво, експеримент се изводи на чистој воденој површини за мерење амплитуде пропадања, а затим се мери пропадање након формирања површинске мембране, а вискозност површинске мембране потиче из разлике између то двоје.
Површинска вискозност је уско повезана са чврстињом површинске мембране, а пошто адсорпциона мембрана има површински притисак и вискозност, мора имати еластичност. Што је веће површински притисак и виши вискозност адсорбоване мембране, то је већи његов еластични модул. Еластични модул површинске адсорпције мембране је важан у процесу стабилизације мехурића.
③ Формирање мицела
Разблаживање решења површински активних средстава поштују законе праћене идеалним решењима. Количина површински активне површине на површини раствора расте са концентрацијом раствора, а када концентрација достигне или пређе одређену вредност, количина адсорпције више не повећава више, а ови вишак молекула површински активно средство у раствору су у раствору на случајној страни. И пракса и теорија показују да формирају удружења у раствору, а ова удружења се називају мицеллес.
Критичка концентрација мицела (ЦМЦ): Минимална концентрација на којој се сурфактанти формирају мицеле у раствору назива се критична концентрација мицела.
④ ЦМЦ вредности заједничких сурфактаната.

ХЛБ је скраћеница баланса хидрофилних липофилних салда, што указује на хидрофилни и липофилни баланс хидрофилне и липофилне групе површински активне, тј. ХЛБ вредност површински активне вредности. Велика ХЛБ вредност означава молекул са јаком хидрофилизацијом и слабом липофилизацијом; обрнуто, јака липофилност и слаба хидрофилација.
① Одредбе ХЛБ вредности
ХЛБ вредност је релативну вредност, па када је ХЛБ вредност развијена, као стандард, ХЛБ вредност парафинског воска, која нема хидрофилни својства, док је ХЛБ вредност натријум додецил сулфата, која је више растворљива вредност од 40 година. Стога је ХЛБ вредност површински активних средстава углавном у опсегу од 1 до 40 година. Генерално гледано у распону од 1 до 40. су липофилни, док су они већи од 10 хидрофилни. Дакле, прекретница од липофилног до хидрофилног је око 10.
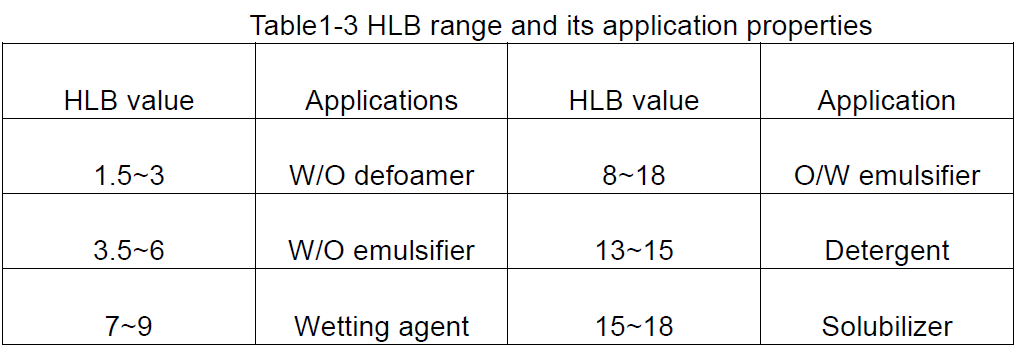
На основу ХЛБ вредности површински активних средстава може се добити општа идеја о њиховим могућим употреби, као што је приказано у Табели 1-3.

Две обострано нерастворљиве течности, једна се расипала у другом као честицама (капљицама или течним кристалима) формирају систем који се зове емулзија. Овај систем је термодинамички нестабилан због повећања граничног подручја две течности када се формира емулзија. Да би се емулзија постала стабилна, потребно је додати трећу компоненту - емулгатор за смањење интерфејске енергије система. Емулгатор припада површински начин, његова главна функција је играње улоге емулзије. Фаза емулзије која постоји капљице назива се распршеном фазом (или унутрашња фаза, дисконтинуирана фаза), а друга фаза која је повезана заједно назива се дисперзијска средња (или спољна фаза, континуирана фаза).
① Емулгатори и емулзије
Заједничке емулзије, једна фаза је вода или водени раствор, друга фаза су органске супстанце које нису мијешете са водом, као што су масти, восак итд. Емулзија формирана у односу на њихову дисперзију у води: Нафта је о / В (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље (уље): В / о (вода / уље). Комплексна вода у уље у води В / О / В тип и уље у уље у / в / о Могу се формирати и више-емулзије.
Емулгатори се користе за стабилизацију емулзија смањењем интерфацијалне напетости и формирањем интерфацијске мембране једноструких молекула.
У емулгацији захтјева за емулгацију:
О: Емулгатор мора бити у могућности да се адсорбује или обогати у интерфејс између две фазе, тако да се умањује интерфацијална напетост;
Б: Емулгатор мора дати честице на оптужбу, тако да је електростатичка одбојност између честица или формира стабилну, високо вискозну заштитну мембрану око честица.
Стога супстанца која се користи као емулгатор мора имати амфифилне групе да би емулгификовале и да сурфактници могу да испуне овај захтев.
② Начини припреме емулзија и фактора који утичу на стабилност емулзија
Постоје два начина за припрему емулзија: Једно је да се користи механичка метода за растрање течности у сићушним честицама у другој течности, која се највише користи у индустрији да би се припремила емулзије; Други је да се течност раствори у молекуларном стању у другој течности, а затим се окупља правилно да формира емулзије.
Стабилност емулзије је способност агрегације против честица која води до раздвајања фазе. Емулзије су термодинамички нестабилни системи са великом слободном енергијом. Стога је такозвана стабилност емулзије заправо време потребно да систем постигне равнотежу, тј. Време потребно за одвајање једне од течности у систему.
Када интерфацијална мембрана са масним алкохолима, масним киселинама и масним аминима и другим поларним органским молекулама, јачина мембране значајно је већа. То је зато што је у интерфацијском адсорпционом слоју молекула и алкохола и алкохола, киселина и амина и других поларних молекула формирало "комплекс", тако да се снага међуфацијске мембране повећала.
Емулгатори који се састоје од више од два сурфактаната називају се мешаним емулгаторима. Мешовито емулгатор адсорбује на интерфејсу воде / уља; Интермолекуларна акција може да формира комплексе. Због снажне интермолекуларне акције, интерфацијална напетост је значајно смањена, количина емулгатора адсорбудирана на интерфејсу је значајно повећана, формирање повезивања интерфацијске густине мембране повећава се снага.
Накнада за течне перлице има значајан утицај на стабилност емулзије. Стабилне емулзије, чије се течне перлице углавном наплаћују. Када се користи јонски емулгатор, Емулгатор ион адсорбован на интерфејсу има своју липофилну групу уметнуте у фазу уља и хидрофилна група је у водоникожној фази, чиме се на терет течност наплаћују. Док се емулзијске перле са истим набојем, одбијају једни друге, а не лако агломерат, тако да је стабилност повећана. Може се видети да више иона емулгатора адвидера на перлицама, што је већа набоја, то је већа могућност спречавања перлица од агломерације, што је стабилнији систем емулзиона.
Вискозност емулзијске дисперзије медија има одређени утицај на стабилност емулзије. Генерално, што је вискост вискозност дисперзног медијума, то је већа стабилност емулзије. То је зато што је вискозитет дисперзивног медија велик, који има снажан утицај на смеђе кретање течних перлица и успорава судара између перлица у течности, тако да систем остаје стабилан. Обично, полимерне супстанце које се могу растворити у емулзијама могу повећати вискозност система и да стабилност емулзија буду веће. Поред тога, полимери такође могу да формирају снажну интерфациалну мембрану, чинећи систем емулзије стабилније.
У неким случајевима, додавање чврстог праха такође може учинити да емулзија има тенденцију да се стабилизује. Чврсти прах је у води, уље или интерфејсу, у зависности од уља, воде на влажном капацитету чврстог праха, ако чврсти прах није потпуно влажан водом, већ и влажном уљем, остаће на води и интерфејсу уља.
Чврсти прах не чини емулзију стабилном јер је прах окупио на интерфејсу, што је слично интерфацијској адсорпцији молекула емулгације, тако да је ближе чврсти материјал прашкастих прашкаран у интерфејсу, то је стабилнија емулзија.
Сурфактанти имају могућност значајног повећања растворљивости нерастворљивог или благо растворљивих органских материја након формирања мицела у воденом раствору, а решење је у то време транспарентно. Овај ефекат Микела назива се солубилизација. Сурфактант који може да произведе растворљивост назива се солубилизатор, а органска материја која се растворљива назива се растворљивом материјом.

Фоам игра важну улогу у процесу прања. Пена је дисперзијски систем у којем се гас диспергује у течној или чврстини, уз гас као распршену фазу и течност или чврст као и дисперзирајући медија, а некада се зове течна пена, док се последња назива чврстим пеном, попут пенасте пластике, пенастог стакла итд.
(1) формирање пене
Пеном овде мислимо овде агрегат мехурића ваздуха одвојен течном мембраном. Ова врста балона увек се брзо диже на течност због велике разлике у густини између дисперзне фазе (гаса) и дисперзијског медија (течности), у комбинацији са ниском вискозности течности.
Процес формирања балона је да се у течност донесе велику количину гаса и мехурићи у течности брзо враћају на површину, формирајући агрегат мехурића одвојених малим количином течног гаса.
ФОАМ има две значајне карактеристике у погледу морфологије: Један је да су мехурићи као распршена фаза често полихедрални облик, то је зато што је на раскрсници мехурића, постоји течност за течни филм да се такси, када у одређеној мери постану течни филм у одређеној мери, то доводи до пукне мехуриће; Друго је да чисте течности не могу формирати стабилну пену, течност која може формирати пену је најмање две или више компоненти. Водени раствори површински активних средстава су типични за системе који су склони генерацији пене и њихова способност генерисања пене такође је повезана са другим својствима.
Сурфактанти са добре снаге пењења називају се средствима за пењење. Иако средство за пењење има добру способност пена, али формирана пена можда неће моћи дуго да одржи дуго времена, односно његова стабилност није нужно добра. Да би се одржала стабилност пене, често у средства за пењање да додате супстанце које могу повећати стабилност пене, супстанца се назива стабилизатор пена, најчешће коришћени стабилизатор је лаурил диетаноламин и додецил диметиламин оксид.
(2) стабилност пене
Фоам је термодинамички нестабилни систем и коначни тренд је да укупна површина течности у систему се смањује након што се мехур поквари и опасну енергију. Процес дефоамирања је процес којим се течна мембрана одваја гас постаје гушћа и разређивача док се не поквари. Стога се степен стабилности пене углавном одређује брзином пражњења течног пражњења и снагом течног филма. Следећи фактори такође утичу на ово.
(3) уништавање пене
Основни принцип уништавања пене је да промени услове који производе пену или да елиминишу стабилизацију фактора пене, тако да постоје и физичке и хемијске методе дефостирања.
Физичко дефомирање значи промјену услова производње пене уз одржавање хемијског састава решења пена, као што су спољне поремећаје, промене температуре или притиска и ултразвучног лечења су све ефикасне физичке методе за уклањање пене.
Метода хемијских дефоамирања је додавање одређених супстанци да комуницира са средством за пењење да смањи чврстоћу течног филма у пени и на тај начин смањује стабилност пене да би се постигла сврха декомирања, такве супстанце се називају дефоамери. Већина дефоамера је површински активна средства. Стога, према механизму дефоамирања, Дефоамер би требао имати снажну способност смањења површинске напетости, једноставан за адсорпцију на површини, а интеракција између површинских молекула адсорпције је слаба, адсорпциони молекули распоређени у отпуштајуће структуре.
Постоје разне врсте дефоамер-а, али у основи су сви неионски сурфактанти. Неинички сурфактанти имају анти-пенасту својства у близини или изнад своје облачне тачке и често се користе као дефоамерс. Алкохоли, посебно алкохоли са граном са гранама, масним киселинама и естерима масних киселина, полиамида, фосфатни естери, силиконска уља итд. Такође се обично користе као одлични дефоамери.
(4) пена и прање
Не постоји директна веза између ефективности пена и прања и количина пене не указује на ефикасност прања. На пример, нонични сурфактанти имају далеко мање својства пењења од сапуна, али њихова деконтаминација је много боља од Спушања.
У неким случајевима пена може бити од помоћи у уклањању прљавштине и прљавштине. На пример, приликом прања посуђа у кући, пена детерџента подиже капљице уља и када пилинг тепихе, пена помаже да се покупи прашину, прах и другу чврсту прљавштину. Поред тога, пена се понекад може користити као показатељ ефикасности детерџента. Будући да масна уља имају ефекат инхибиције на пену детерџента, када има превише нафте и премало детерџента, није генерисана пена или ће се оригинална пена нестати. ФОАМ се такође може понекад користити као показатељ чистоће испирања, јер је количина пене у раствору исперења тенденција да се смањи са смањењем детерџента, тако да се количина пене може користити за процену степена испирања.
У ширем смислу, прање је процес уклањања нежељених компоненти од објекта који се пере и постигне одређену сврху. Прање у уобичајеном смислу односи се на поступак уклањања прљавштине са површине носача. У прању је интеракција између прљавштине и превозника ослабљена или елиминисана дејством неких хемијских супстанци (нпр. Детерџент итд.), Тако да се комбинација прљавштине и превозника мења у комбинацију прљавштине и детерџента, и коначно је прљавштина одвојена од носача. Док се објекти за прање и уклањање прљавштине су разнолики, прање је веома сложен процес и основни процес прања може се изразити у следећим једноставним односима.
Царрие ·· Дирт + Детерџент = Царриер + Дирт · Детерџент
Процес прања се обично може поделити у две фазе: Прво, под дејством детерџента, прљавштина је одвојена од свог носача; Друго, самостојећа прљавштина се распршена и суспендована у медијуму. Процес прања је реверзибилни процес, а прљавштина се распршена и суспендована у медијума се такође може преносити са медија на објект који се испере. Стога би добар детерџент требао имати могућност растјерања и суспендовања прљавштине и спречило да се преправите прљавштину, поред могућности уклањања прљавштине од превозника.
(1) Врсте прљавштине
Чак и за исти предмет, врста, састав и количина прљавштине могу се разликовати у зависности од животне средине у којој се користи. Прљавштина нафте углавном је нека животињска и биљна уља и минерална уља (као што су сирове нафте, уље гориво, уље, чврсти прљавштину је углавном части, пепео, рђа, угљеник Црна итд. У погледу одеће, у погледу од одеће, постоји прљавштина, као што је људско тело, итд.; прљавштина од хране, као што су воћни мрље, кување нафтних мријека, мрље за промет, скроб итд.; прљавштина са козметике, као што је руж, лак за нокте, итд.; прљавштина из атмосфере, као што је чађа, прашина, блато итд.; Други, као што су мастило, чај, премаз итд. Долази у разним врстама.
Различите врсте прљавштине обично се могу поделити у три главне категорије: чврста прљавштина, течна прљавштина и посебна прљавштина.
① чврста прљавштина
Заједничка чврста прљавштина укључује честице пепела, блата, земље, рђе и угљеника црне боје. Већина ових честица има електричну накнаду на њиховој површини, већина њих се негативно наплаћује и може се лако адсорбирати на предметима влакана. Чврста прљавштина је опћенито тешко растворити у води, али се може распршити и суспендовати детерџентским решењима. Чврсти прљавштина са мањом масом је теже уклонити.
② Течна прљавштина
Течна прљавштина је углавном растворљива у нафту, укључујући биљне и животињске уље, масне киселине, масне алкохоле, минерална уља и њихове оксиде. Among them, plant and animal oils, fatty acids and alkali saponification can occur, while fatty alcohols, mineral oils are not saponified by alkali, but can be soluble in alcohols, ethers and hydrocarbon organic solvents, and detergent water solution emulsification and dispersion. Течна прљавштина растворљива уља углавном има снажну силу са предметима влакана и чврсто је адсорбована на влакнима.
③ Специјална прљавштина
Посебна прљавштина укључује протеине, скроб, крв, људске секреције као што су зној, себум, урин и воћни сок и чајни сок. Већина ове врсте прљавштине може се хемијски и снажно адсорбирати на предметима влакана. Стога је тешко опрати.
Различите врсте прљавштине ретко се налазе сами, али често се мешају заједно и адсорбују на објект. Прљавштина се понекад може оксидовати, раздвојити или пропети под спољним утицајима, стварајући тако нову прљавштину.
(2) адхезија прљавштине
Одећа, руке итд. Може се обојити јер постоји нека врста интеракције између објекта и прљавштине. Прљавштина се придржава објектима на различите начине, али нема више од физичких и хемијских адхезија.
①Подавање чађе, прашине, блата, песка и дрвеног угља за одећу је физичко пријањање. Генерално гледано, кроз ову адхезију прљавштине, а улога између обојеног објекта је релативно слаба, уклањање прљавштине је такође релативно лако. Према различитим снагама, физичко пријањање прљавштине може се поделити на механичко адхезијско и електростатичко пријањање.
О: Механичко адхезија
Ова врста лепка углавном се односи на пријањање неке чврсте прљавштине (нпр. Прашина, блато и песак). Механичко пријањање је један од слабијих облика лепљења прљавштине и може се уклонити готово чисто механичким средствима, али када је прљавштина мала (<0,1УМ), теже је уклонити.
Б: Електростатичко адхезија
Електростатичко пријањање углавном се манифестује у деловању честица прљавих прљавштина на супротно набијеним објектима. Већина влакнастих објеката негативно се наплаћује у води и лако се може придржавати одређене позитивно набијене прљавштине, попут типова лимета. Неке прљавштине, иако негативно оптужени, попут угљених црних честица у воденим решењима, могу се придржавати влакана кроз јонске мостове (јони између вишеструких супротности са њима, дјеловати заједно са њима на начин на сличан мостовима) формираним позитивним јонима у води (нпр.
Електростатичка акција је јача од једноставне механичке акције, чинећи уклањање прљавштине релативно тешко.
② Хемијска адхезија
Хемијска адхезија односи се на феномен прљавштине која делује на објект хемијским или водоничним везама. На пример, поларни чврсти прљавштини, протеински, рђа и друга пријања на предметима влакана, влакна садрже карбоксил, хидроксил, амид и друге групе, ове групе и масне масне киселине, масни алкохоли су лако формирати обвезнице водоника. Хемијске снаге су углавном снажне, а прљавштина је, дакле, чвршће везана за објект. Ову врсту прљавштине је тешко уклонити уобичајеним методама и захтијевати посебне методе да се баве њом.
Степен адхезије прљавштине односи се на природу самог прљавштине и природу објекта на који се придржава. Генерално, честице се лако придржавају влакнастих предмета. Што је мања текстура чврсте прљавштине, јачи лепљење. Полар прљавштина на хидрофилним објектима попут памука и стакла придржавају се снажније од непарске прљавштине. Неполарна прљавштина се снажнија придржава више од поларне прљавштине, као што су поларне масти, прашине и глине и мање је једноставне за уклањање и чишћење.
(3) Механизам за уклањање дирта
Сврха прања је уклањање прљавштине. У медију одређене температуре (углавном воде). Користећи различите физичке и хемијске ефекте детерџента да ослаби или отклони ефекат прљавштине и опране објекте, под радњама одређених механичких сила (као што је ручно трљање, агитација прања машина, тако да је прљавштина и опрати објекте из сврхе деконтаминације.
① Механизам уклањања течног прљавштине
О: Влажење
Течно запрљано је углавном засновано на уље. Уље мрље влажне најплозне предмете и рашири се мање или мање као нафтни филм на површини влакнасте материјале. Први корак у акцији прања је влажење површине течношћу за прање. Ради илустрације, површина влакана се може сматрати глатком чврсте површине.
Б: Одреди нафте - механизам за цурлинг
Други корак у акцији прања је уклањање нафте и масти, уклањање течне прљавштине постиже се врстама намотаности. Течна прљавштина првобитно је постојала на површини у облику раширеног уљаног филма и под преференцијалним утицајем течности прања на чврстој површини (тј. Површина влакана), увијена је у нафтне перлице корак по корак, који су замењени течношћу за прање и на крају су напустили површину под одређеним спољним силама.
② Механизам уклањања чврсте прљавштине
Уклањање течне прљавштине углавном је преко преференцијалног влажења носача прљавштине прањем раствором прање, док је механизам за уклањање чврсте прљавштине различито, где је процес прања углавном о влажењу масе прљавштине и њену површину за прање. Због адсорпције површински активних средстава на чврстим прљавштини и њеној носионици, интеракција између прљавштине и површине се смањује и да је чврстоћа масе прљавштине на површини смањена, па се маса прљавштина лако уклања са површине носача.
Поред тога, адсорпција површински активних средстава, посебно јонских површински активних средстава, на површини чврсте прљавштине и њеног превозника има потенцијал да повећа површински потенцијал на површини чврсте прљавштине и њеног превозника, што је више погодније за уклањање прљавштине. Чврсти или опћенито влакнасте површине обично се негативно наплаћују у воденим медијима и стога могу формирати дифузне двоструке електронске слојеве на масама прљавштине или чврсте површине. Због одбојности хомогених оптужби, пријањање честица прљавштине у води до чврсте површине је ослабљено. Када се дода анионски сурфактант, јер истовремено може да повећа негативни површински потенцијал честица прљавштине и чврсте површине, одбојност између њих је побољшана, јачина лепљења честица је смањена, а прљавштина је лакше уклонити.
Неинички сурфактанти се адсорбира на опште опуњеној чврстим површинама и иако не мењају значајно међусобни потенцијал, адсорбовани нејунички сурфактни материјали имају тенденцију да формирају одређену дебљину адсорбованог слоја на површини која помаже у спречавању да се спречи успостављање прљавштине.
У случају катионских површински активних средстава, њихова адсорпција смањује или елиминише негативни површински потенцијал масе прљавштине и његову површину носача, што смањује одбојност између прљавштине и површине и стога не погодује уклањању прљавштине; Поред тога, након адсорпције на чврстим површинама, катионски сурфактанти имају тенденцију да окрећу чврсту површинску хидрофобну и стога не доприносе површинским влажним и стога прање.
③ Уклањање посебних тла
Протеин, скроб, људски сечи, воћни сок, чајни сок и други такву прљавштину тешко је уклонити нормалним површински активним актима и захтевају посебан третман.
Мрље протеина као што је крема, јаја, крв, млеко и коже изрезу имају тенденцију да се кокуларају на влакнима и дегенерацији и постају јачи пријањање. Затезање протеина може се уклонити коришћењем протеастина. Ензимски протеасе разграђује протеине у прљавштини у аминокиселине растворљиве у води или олигопептиди.
Мрље скроба углавном потичу из прехрамбених производа, као што су грави, лепљење итд. Амилаза има каталитички ефекат на хидролизу мрља шкроба, узрокујући да се шкроб провали у шећере.
Липаза катализује распадање триглицерида, што је тешко уклонити нормалним методама, као што су себум и јестиво уља и сломе их у растворљиви глицерол и масним киселинама.
Неке обојене мрље од воћних сокова, чајашки сокови, мастила, ружа итд. Често је тешко чистити темељно чак и након поновљеног прања. Ове мрље се могу уклонити редокс реакцијом са оксидацијом или редукционом агенсом као што је избељивачи, која уништава структуру боју који стварају или пуне групе за производњу боја или у боји и деградира их у мање водене компоненте у води.
(4) Механизам уклањања мрља за хемијско чишћење
Горе је заправо за воду као медиј прања. У ствари, због различитих врста одеће и структуре, нека одећа која користи прање воде није прикладна или није лако оперивати чисту одећу након прања и чак деформације, итд., Итд. Опрема вуне производи се такође често појављују феномен скупљања, неки вунени производи са прањем воде је такође лако питати, променити боје; Неки се свили сви свиле осећају горе након прања и изгубећи сјај. За ову одећу често користите метод сувог чишћења за деконтаминирање. Такозвано хемијско чишћење углавном се односи на метод прања у органским растварачима, посебно у непарним растварачима.
Хемијски чишћење је нежнији облик прања од прања воде. Будући да хемијско чишћење не захтева много механичке акције, не узрокује оштећења, наборано и деформација за одећу, док средства за хемијско чишћење, за разлику од воде, ретко производе ширење и контракцију. Све док се технологија правилно рукује, одећа може бити сува очишћена без изобличења, бледило у боји и продужени радни век услуга.
У погледу хемијског чишћења, постоје три широке врсте прљавштине.
①Оил-растворљива прљавштина растворљива уљана уљана укључује све врсте нафте и масти, која је течна или масна и може се растворити у растварачима хемијског чишћења.
②Вватер растворљива прљавштина растворљива у растворљивој води је растворљива у воденим растворима, али не и у сувом средствима за чишћење, адсорбује се на одећи у воденој држави, вода испарава након падавина грануларних чврстих материја, као што су и неорганске соли, скроб, протеин итд.
Ооил анд Водено нерастворљива прљавштина уља и вода нерастворљива није растворљива у води нити растворљива у растварачима за хемијске чишћење, попут угљених црнаца, силицијатива различитих метала и оксида итд.
Због различите природе различитих врста прљавштине, постоје различити начини уклањања прљавштине у процесу хемијског чишћења. Уљана растворљива уља, као што су животињска и биљна уља, минерална уља и масти, лако се растворују у органским растварачима и могу се лакше уклонити у хемијском чишћењу. Одлична растворљивост растварача за хемијско чишћење уља и масти у основи долази из зидова Ван дер-а између молекула.
За уклањање воде растворљиве у води као што су неорганске соли, шећери, протеини и зноји, такође се мора додати праву количину воде и на иначе да је у супротном тешко уклонити водоотпорни прљавштину. Међутим, тешко је растворити у средством за чишћење сувог чишћења, тако да повећате количину воде, такође морате да додате површински активне материје. Присуство воде у средством за чишћење сувог чишћења може направити површину хидрираног прљавштине и одеће, тако да је лако комуницирати са поларним групама површински активних средстава, што погодује адсорпцији површински активних средстава на површини. Поред тога, када сурфактанти формирају мицеле, торбица растворљива у води и вода могу се растворити у мицеле. Поред повећања садржаја воде растварача за хемијско чишћење, површински активни материјали такође могу да играју улогу у спречавању поновног уклањања прљавштине да побољша ефекат деконтаминације.
Присуство мале количине воде је неопходно за уклањање водотопљиве прљавштине, али превише воде може проузроковати изобличење и боцање у неку одећу, тако да количина воде у средствима за хемијско чишћење мора бити умерена.
Прљавштина која није ни растворљива у води и растворљива у нафту, чврсте честице попут пепела, блата, земље и угљеника, углавном се причвршћују на одећу електростатичких снага или у комбинацији са уљем. У хемијском чишћењу, проток растварача, утицај може учинити електростатичкој снажној адсорпцији прљавштине, а средство за чишћење сува може растворити уље, тако да је комбинација нафте и прљавштине и причвршћена на одећу чврстих честица у малу количину воде и површински активирање, тако да они са чврстим честицама за чишћење и површински активирају, тако да они са чврстих честица прљавштине могу бити стабилно огибљење, тако да они са чврстих честица прљавштине могу бити стабилно огибљење, тако да они са чврстих честица прљавштине могу бити стабилно огибљење, тако да они са чврстих честица прљавштине могу бити стабилно огибљење, тако да оне са чврстих честица прљавштине могу бити стабилно ошишање.
(5) Фактори који утичу на акцију прања
Смјер адсорпције површински активних средстава на интерфејсу и смањење површине (интерфацијалне) напетости главни су фактори у уклањању течности или чврсте прљавштине. Међутим, процес прања је сложен и ефекат прања, чак и са истим типом детерџента, под утицајем многих других фактора. Ови фактори укључују концентрацију детерџента, температуре, природу прљања, врсте влакана и структуре тканине.
Концентрација површински активне површине
Мицела површински активних средстава у раствору играју важну улогу у процесу прања. Када концентрација достигне критичну концентрацију мицела (ЦМЦ), ефекат прања расте нагло. Стога концентрација детерџента у растварачу треба да буде већа од вредности ЦМЦ-а да би се добри ефекат прања. Међутим, када је концентрација површински активне мјери већа од вредности ЦМЦ-а, инкрементално повећање ефекта прања није очигледно и није потребно повећати концентрацију површински активне атракције.
Приликом уклањања нафте растворљивом, ефекат растворљивости расте са повећањем концентрације површински активне површине, чак и када је концентрација изнад ЦМЦ-а. У то време је препоручљиво користити детерџент на локално централизовани начин. На пример, ако има пуно прљавштине на лисици и овратника одеће, слој детерџента се може применити током прања да бисте повећали растворни ефекат површински активне боје на уље.
②Температуре има веома важан утицај на акцију деконтаминације. Генерално, повећање температуре олакшава уклањање прљавштине, али понекад превисока температура такође може изазвати недостатке.
Повећање температуре олакшава дифузију прљавштине, чврста маст се лако емулдификује на температурама изнад њене тачке топљења и влакна се повећавају у отеклинику због повећања температуре, а све олакшавају уклањање прљавштине. Међутим, за компактне тканине, микрогапови између влакана се смањују као влакна која се шире, што је штетно за уклањање прљавштине.
Промјене температуре такође утичу на растворљивост, вредност ЦМЦ и мицелле величине површински активних средстава, на тај начин утицала на ефекат прања. Растворљивост сурфактаната са дугим ланцима угљеника је ниска на ниским температурама, а понекад је растворљивост још нижа од вредности ЦМЦ-а, тако да температура прања треба прикладно поставити на одговарајући начин. Ефекат температуре на Вредност ЦМЦ-а и мицелле величине је различит за јонске и неионске површински активне материје. За јонске површински активне површине, повећање температуре углавном повећава вредност ЦМЦ-а и смањује величину мицела, што значи да би се требала повећати концентрација површински активне материје у раствору прања. За неонске површински активне материје, повећање температуре доводи до смањења вредности ЦМЦ-а и значајно повећање јачине мицела, тако да је јасно да ће одговарајуће повећање температуре помоћи нејинском сурфактану да изврши свој површински активни ефекат. Међутим, температура не сме прелазити његову облачну тачку.
Укратко, оптимална температура прања зависи од формулације детерџента и објекта се испере. Неки детерџенти имају добар ефекат детерџента на собној температури, док други имају много различита детерџента између хладног и врућег прања.
③ пена
Уобичајено је збунити моћ пењења са ефектом прања, верујући да детерџенти са великом снагом пенасти имају добар ефекат прања. Истраживање је показало да нема директног односа између ефекта прања и количине пене. На пример, прање са ниским детерџентима за пенање није мање ефикасно од прања са високим детерџентима за пењење.
Иако пена није директно повезана са прањем, постоје прилика када помаже у уклањању прљавштине, на пример, приликом прања посуђа ручно прање посуђа. Приликом пилинг тепиха, пена се такође може одузети прашину и друге чврсте прљаве честице, чишћење тепиха за велики удео прашине, па средства за чишћење тепиха треба да имају одређену способност пењене.
Снага пењења је такође важна за шампоне, где је фина пена произведена течношћу током шампонирања или купаћим купањем, осећај косе подмазан и удобан.
④ Сорте влакана и физичка својства текстила
Поред хемијске структуре влакана, који утиче на пријањање и уклањање прљавштине, појава влакана и организација пређе и тканине утиче на лаковање уклањања прљавштине.
Ваге вунене влакна и закривљене равне траке памучних влакана је вероватније да ће акумулирати прљавштину од глатких влакана. На пример, угљеник Црно обојено на целулозним филмовима (вискозни филмови) је једноставан за уклањање, док је угљен црно обојено на памучним тканинама тешко испрати. Други пример је да су тканине за краткорочне влакне од полиестера више склоније акумулирајући мрље од дугог влакана, а нафтне мрље на тканинама за краткорочне влакна такође је теже уклонити од нафтних флека на малим влакнима.
Чврсто искривљене пређе и утешке тканине, због малог јаза између влакана могу се одупријети инвазији прљавштине, али исто такође може да спречи и течност за прање да искључи унутрашњу прљавштину, тако да уске тканине почну да се опире добрим прљавштином.
⑤ Тврдоћа воде
Концентрација ЦА2 +, МГ2 + и других металних јона у води има велики утицај на ефекат прања, посебно када се анионски сурфактници сусрећу са ЦА2 + и МГ2 + јони који формирају калцијум и магнезијум соли који су мање растворљиви и смањиће њену детерденцију. У тврдој води, чак и ако је концентрација површински активне материје висока, детерџент је још много горе него у дестилацији. Да би се површински активно појавио најбољи ефекат прања, концентрација ЦА2 + јона у води треба смањити на 1 к 10-6 мол / л (ЦАЦО3 на 0,1 мг / л) или мање. Ово захтева додатак различитих омекшивача до детерџента.
Вријеме поште: 25. фебруара



